








《物理化学界面现象PPT课件下载》是由用户上传到老师板报网,本为文库资料,大小为1016.96 KB,总共有27页,格式为pptx。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 27页
- 1016.96 KB
- VIP模板
- pptx
- 数字产品不支持退货
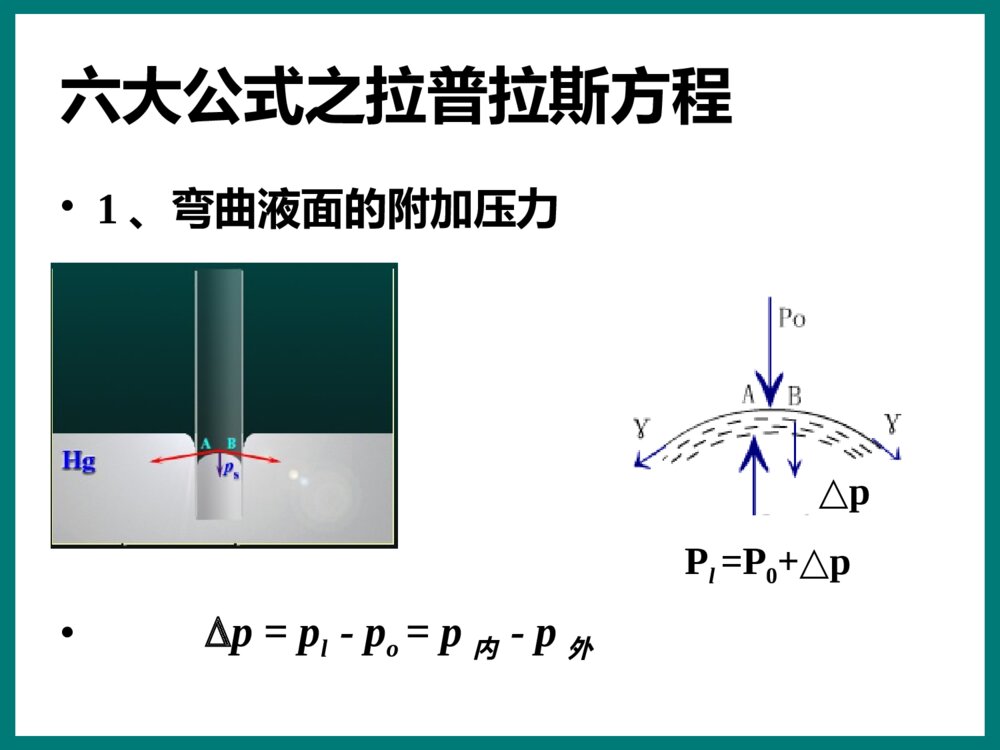
界面现象小结研究的主要问题?产生界面(表面)现象的原因是什么?重点知识“非常6+1”6→六个公式1→一个概念一个概念之表面张力1、几个铺垫概念:①界面:所有两相的接触面②表面:与气体接触的界面③比表面积:物质表面积与其质量之比或表面积与其体积之比,是物质分散程度的度量。s//SssaAmaAV或s//SssaAmaAV或一个概念之表面张力•2、定义:•沿着与液面相切方向垂直作用于分界线的单位长度上的紧缩力。用•3、方向:•对于平液面,表面张力与液面平行且垂直作用于分界线上;•对于弯曲液面,表面张力与液面相切且垂直作用于分界边缘。一个概念之表面张力4、实质:紧缩力,使表面积减少的紧缩力。5、产生的原因:液体表面的分子受力不对称。6、表面张力、表面功及表面吉布斯函数的关系:三者的数值、量纲等同,但它们有不同的物理意义,是从不同角度说明同一问题。δWr’/dAs=,,sTpNGA,,sTpNGA一个概念之表面张力•7、影响表面张力的因素:•①与物质的本性有关,分子间作用力越大,表面张力越大。一般,对于液体表面有:•>离子键)>(极性键)>•②与温度有关•一般的,温度越高,表面张力越小。一个概念之表面张力•③压力:•a、表面分子手里不对称程度•p↑b、气体分子可悲表面吸附,•c、气体分子溶于液相•④与接触相的性质有关•⑤与分散度、运动情况等有关。六大公式之拉普拉斯方程•1、弯曲液面的附加压力•p=pl-po=p内-p外△pPl=P0+p△六大公式之拉普拉斯方程说明:r是弯曲液面的曲率半径①该形式的Laplace公式适用于球形液面。②曲面内(凹)的压力大于曲面外(凸)的压力,Δp>0。③r越小,Δp越大;r越大,Δp越小。对平液面:r→∞,Δp→0(并不是=0)④Δp方向:永远指向球心。2方程pLaplacer2方程pLaplacer六大公式之“求高”方程毛细现象r是毛细管半径显然,h>0时,液面上升;(能润湿)h<0时,液面下降。(不能润湿)2coshrg2coshrg六大公式之开尔文公式r是弯曲液面的曲率半径讨论:(1)对于纯液体,在一定温度下,r),且,。(2)凸液面,凹液面,2ln公式rpMKelvinpRTr0,ln0rrprppp0,ln0rrprppp2ln公式rpMKelvinpRTr0,ln0rrprppp0,ln0rrprppp六大公式之开尔文公式四种亚稳状态及新相的生成1、过饱和蒸气:2、过热液体:3、过冷液体:4、过饱和溶液:讨论:1、附加压力产生的原因?•因为液体的表面张力。•2、表(界)面张力仅液体表面才有?•界面张力的产生原因:界面层分子受力不对称。固体表面、液液界面、液固界面等都有表面张力。•3、固体的表面张力会使固体有怎样的表面现象?六大公式之朗格缪尔等温吸附式1、吸附•①定义:在固体或液体表面,某种物质的浓度与体相浓度不同的现象称为吸附•②分类:•A、物理吸附•B、化学吸附性质物理吸附化学吸附吸附力范德华力化学键吸附层数单层或多层单层吸附热小(近于液化热)大(近于反应热)选择性无或很差较强可逆性可逆不可逆吸附平衡易达到不易达到六大公式之朗格缪尔等温吸附式•2、吸附量•①定义:当吸附达平衡时,每克吸附剂吸附的吸附质。•②公式:•等温吸附•等压吸附•等量吸附mnnaaVVm(,)fTPmnnaaVVm(,)fTP六大公式之朗格缪尔等温吸附式••Va为吸附体积,为吸满单分子层的体积•b—吸附系数或吸附平衡常数,与吸附剂、吸附质、T有关。b值大,吸附能力大amaVVamVamamaVpbVVp1amaVVamVamamaVpbVVp1六大公式之朗格缪尔等温吸附式•公式的应用amamaVpbVVp1amaVbpVp及求由直线的斜率与截距可图为一直线作,比表面积可进一步计算吸附剂的由amVmamsLaVVa0)()101C01)/(/20032makPamolVkgmVkgmamams吸附分子的截面积下的体积,气体在标准状况(饱和吸附量吸附剂的比表面积amamaVpbVVp1amaVbpVp及求由直线的斜率与截距可图为一直线作,比表面积可进一步计算吸附剂的由amVmamsLaVVa0)()101C01)/(/20032makPamolVkgmVkgmamams吸附分子的截面积下的体积,气体在标准状况(饱和吸附量吸附剂的比表面积六大公式之朗格缪尔等温吸附式•4、吸附热•吸附是自发过程,<0,吸附过程中,气体分子由三维空间被吸附到二维表面,自由度减少,分子的平动受到限制,所以。即吸附通常为放热反应。•摩尔吸附焓adsHm:恒温、恒压和恒定吸附剂表面积时吸附1mol气体的热效应。STGHSTHGSTGHSTHG六大公式之杨氏方程1、润湿角:固液界面的水平线与气液界面在O点的切线之间的经过液相的夹角2、杨氏方程l-gs-ls-gcosgslsglcosgslsgl六大公式之杨氏方程3、润湿现象4、润湿现象的应用①防水衣料的改良)1cos\'a(沾湿:lWcos\'liW浸湿:cos1)lS铺展:(-180\'090\'000aiWWS)1cos\'a(沾湿:lWcos\'liW浸湿:cos1)lS铺展:(-180\'090\'000aiWWS六大公式之吉布斯吸附等温式1、溶液表面的吸附溶质在溶液表面层中的浓度与在溶液本体中浓度不同的现象。2、表面过剩(表面吸附量)在单位面积的表面层中,所含溶质的物质的量与同量溶剂在溶液本体中所含溶质物质的量的差值。六大公式之吉布斯吸附等温式2、公式:稀溶液--c为溶质在本体中的平衡浓度;浓溶液--c用活度a表示。cdRTdccdRTdc六大公式之吉布斯吸附等温式cdRTdc γⅠⅡⅢcⅠ--负吸附;Ⅱ、Ⅲ--正吸附。cdRTdc六大公式之吉布斯吸附等温式3、表面活性剂•①定义:加入少量就能显著降低溶液表面张力的一类物质,通常是指降低水的表面张力。阴离子型•②分类:离子型阳离子型•表面活性剂两性型•非离子型•③HLB法(了解)产生界面(表面)现象的原因是?•各界面(表面)现象:•1、气液表面:附加压力(拉、开、高)•2、气固表面:吸附(朗格缪尔)•3、固液界面:润湿(杨氏)•4、溶液表面:表面过剩(吉布斯)•表面张力谢谢大家!



















